ISO 17100 - MDR & IVDR sind auf dem Weg

Sicherheitsvorteile der ISO 17100 – aktuell und zukünftig
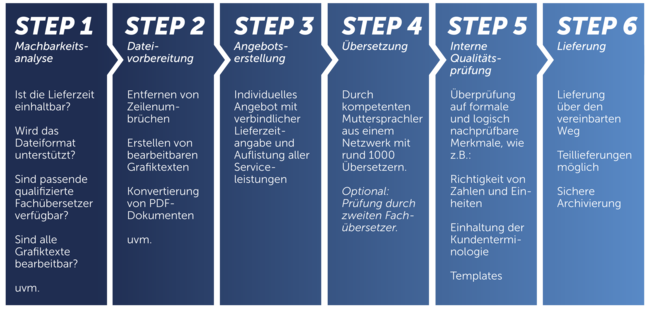
mt-g steht für einwandfreie medizinische und pharmazeutische Fachübersetzungen. Dies gelingt uns unter anderem durch klar definierte Prozesse entlang der kompletten Übersetzungskette. Ein Grundbaustein unseres Qualitätsmanagements ist der Anspruch der internationalen Norm DIN EN ISO 9001.
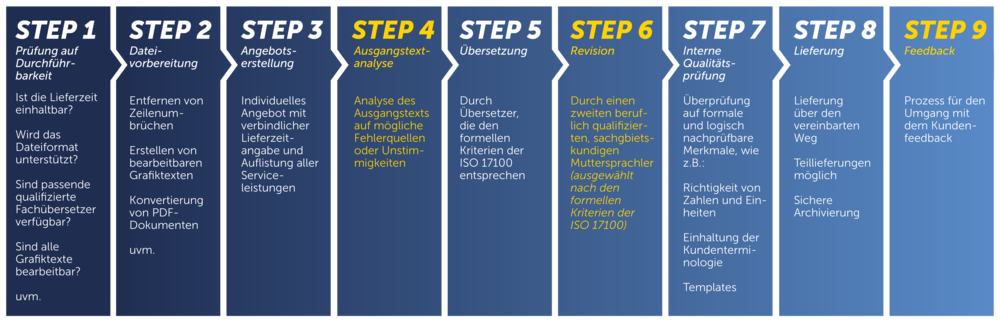
Eine Übersetzung nach der DIN EN ISO 17100 zu strukturieren steigert die Qualität durch noch höhere Qualifikations- und Fachkompetenzanforderungen und gibt Ihnen – nicht nur hinsichtlich der anstehenden MDR- und IVDR-Verordnungen– zusätzliche Sicherheit gegenüber dem herkömmlichen Übersetzungsprozess. Der weltweite Standard wirkt sich generell positiv auf Ihre Audits aus.
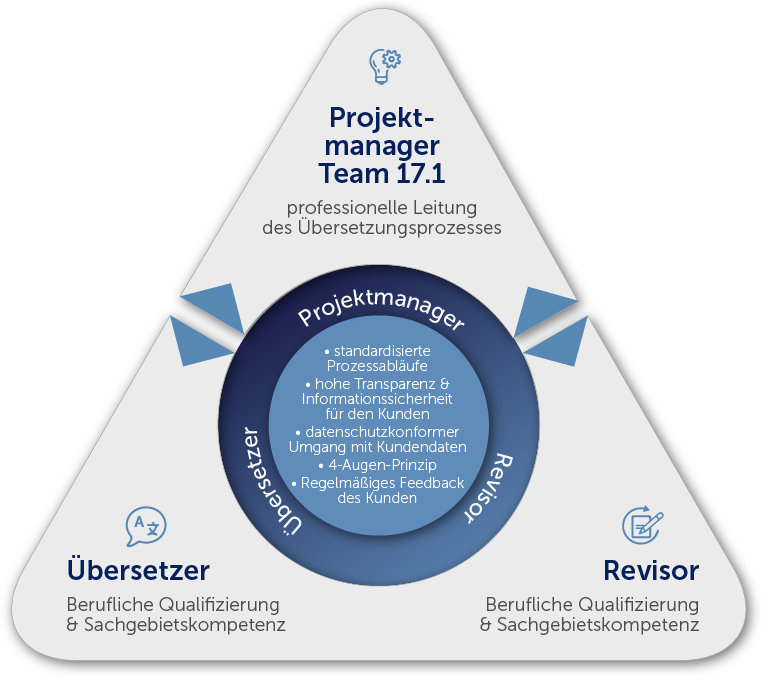
Übersetzer & Revisoren
- anerkannter Abschluss einer Hochschule auf dem Gebiet des Übersetzens oder
- anerkannter Abschluss einer Hochschule auf einem anderen Gebiet plus zwei Jahre Vollzeit-Berufserfahrung im Übersetzen oder
- fünf Jahre Vollzeit-Berufserfahrung auf dem Gebiet des Übersetzens plus Erfahrung in dem zu übersetzenden oder redigierenden Fachgebiet
Projektmanager
- Kompetenz bei der Organisation und Unterstützung des Übersetzungsprozesses
- kontinuierliche Weiterbildung der Projektmanager
Ab 26. Mai 2021 gilt die neue Medizinprodukteverordnung MDR (Medical Device Regulation 2017/745). Ab dem 26. Mai 2022 gilt die In-vitro-Diagnostika-Verordnung (IVDR) der Europäischen Union. Mit diesen Verordnungen werden die Anforderungen an Hersteller von Medizinprodukten verschärft – auch in sprachlicher Hinsicht bezüglich Übersetzung und Lokalisierung. Sämtliche Übersetzungsprozesse müssen beherrscht werden, da sichergestellt sein muss, dass Übersetzungen »korrekt und auf dem neuesten Stand« (Art. 16 MDR und Art. 16 IVDR) sind.
Der Verständlichkeit und Präzision von Übersetzungen wird also noch mehr Bedeutung zukommen – in bis zu 24 Sprachen. Übersetzungsprozesse nach ISO 17100 geben Ihnen, Ihren Kunden und Ihren benannten Stellen die Sicherheit, konforme Übersetzungen zu erhalten.
Uns ist bewusst, dass Sie, als Hersteller von medizinischen Produkten, für die Gesundheit und Sicherheit Ihrer Kunden verantwortlich sind und dass die Übersetzungen – seien es Packungsbeilagen, Beschriftungen oder Webtexte – Produktbestandteile sind. Daher können Sie die größte Sorgfalt bei der Erstellung dieser Übersetzungen erwarten.
Wir arbeiten auschließlich mit fachkundigen Übersetzern zusammen, die kundenspezifische Terminologie, Wording des Unternehmens und spezifische Vorgaben in ihren Texten übernehmen und diese zusammen mit ihren Übersetzungen in Datenbanken, den Translation Memory Systemen, speichern. Dieses trägt dazu bei, dass konsistente Übersetzungen und Fachtermini in weiteren Texten eingehalten werden. Durch eine langfristige Zusammenarbeit werden nach und nach Übersetzungskosten gesenkt. Wording und Terminologie werden sukzessive verfeinert.